Se il messaggio non viene visualizzato correttamente clicca qui per consultare la versione online >>
|
||
 |
||
|
||
Contenuti
|
||
Regimi iniettabili ad azione prolungata per il trattamento dell'HIV e per la PrEP | ||
 Carlos del Rio, Diane Havlir, Charles Flexner, Francois Venter, Hyman Scott, Nittaya Phanuphak (dall'alto al basso e da sinistra a destra) a CROI 2021. | ||
|
Alla Conferenza su Retrovirus e Infezioni Opportunistiche (CROI 2021), svoltasi anche quest’anno in edizione virtuale, una tavola rotonda ha affrontato il tema dei regimi iniettabili, sottolineando quanto sia importante che siano pratici e convenienti. Secondo la prof.ssa Diane Havlir, se nello scorso decennio i progressi in materia di trattamento dell'HIV sono stati principalmente rappresentati dall’impiego di potenti inibitori dell'integrasi e dai regimi monocompressa, il prossimo decennio sembra avviato ad essere l'era dei regimi ad azione prolungata. Il prof. Francois Venter ha riferito che in Sudafrica c'è grande entusiasmo per questi farmaci long acting da parte dei pazienti: la loro introduzione presenta però delle difficoltà che destano più di una preoccupazione tra gli operatori sanitari. Nel paese è infatti attivo il programma per l’offerta di trattamento antiretrovirale più ampio al mondo, e adottando i regimi iniettabili si renderebbe necessario ripensare tutto il flusso di lavoro nei centri che erogano i trattamenti, già oberati di lavoro. Venter si è invece detto più aperto rispetto al loro impiego nella profilassi pre-esposizione (PrEP), nell’ambito di cui potrebbero effettivamente rappresentare un vantaggio, dato il numero limitato di persone che finora assumono la PrEP per via orale. Il primo farmaco a lunga durata d’azione per la PrEP, il cabotegravir in formulazione iniettabile, potrebbe già essere immesso nel mercato entro la fine di quest'anno o all'inizio dell’anno prossimo. Ancora non si hanno informazioni circa i costi. Un’analisi presentata a CROI 2021 dalla dott.ssa Anne Neilan del Massachusetts General Hospital ha calcolato che negli Stati Uniti, per essere conveniente, il farmaco dovrebbe costare meno della metà del prezzo di listino (massimo) per la combinazione iniettabile cabotegravir /rilpivirina Cabenuva, già autorizzata per il trattamento dell'HIV. Per essere più conveniente rispetto alla combinazione tenofovir disoproxil fumarato/emtricitabina (TDF/FTC) in versione generica (che negli Stati Uniti costa 8300 dollari l'anno), il cabotegravir iniettabile (CAB-LA) dovrebbe costare non più di 11.600 dollari. A questo prezzo, costerebbe poco meno di 100.000 dollari per ogni anno di vita guadagnato ponderato in funzione della qualità della vita – la cifra massima a cui un intervento è di solito considerato conveniente negli Stati Uniti. In Europa e in altri paesi del mondo, il TDF/FTC in versione generica può essere acquistato a cifre che sia aggirano tra i 300 e i 900 dollari l'anno. Sebbene questo dato non sia stato analizzato da Neilan e colleghi, a fronte della superiore efficacia preventiva del cabotegravir ad azione prolungata, secondo il modello potrebbe comunque essere conveniente in termini di costo-efficacia o garantire un risparmio nel lungo termine nel contesto europeo, ma solo se costasse intorno ai 2000-3000 dollari l'anno. L'Agenzia europea per i medicinali (EMA) ha approvato questa combinazione iniettabile nel dicembre 2020, sia per un regime che prevede una somministrazione mensile che per quello che ne prevede una ogni due mesi. Gli enti regolatori di Stati Uniti e Canada (dove i due farmaci iniettabili sono commercializzati unitamente con il nome di Cabenuva) hanno invece approvato solo il regime mensile. Lo studio ATLAS-2M ha preso in considerazione 1045 partecipanti, che sono stati randomizzati per ricevere iniezioni di 400mg di cabotegravir e 600mg di rilpivirina ogni quattro settimane oppure 600mg di cabotegravir e 900mg di rilpivirina ogni otto settimane. Dopo due anni hanno mantenuto la soppressione virale il 90,2% dei partecipanti a cui veniva somministrata un’iniezione al mese e il 91,0% di quelli a cui veniva invece somministrata una volta ogni due mesi. | ||
La ‘resilienza’ dei programmi HIV in Africa durante la pandemia da COVID-19 | ||
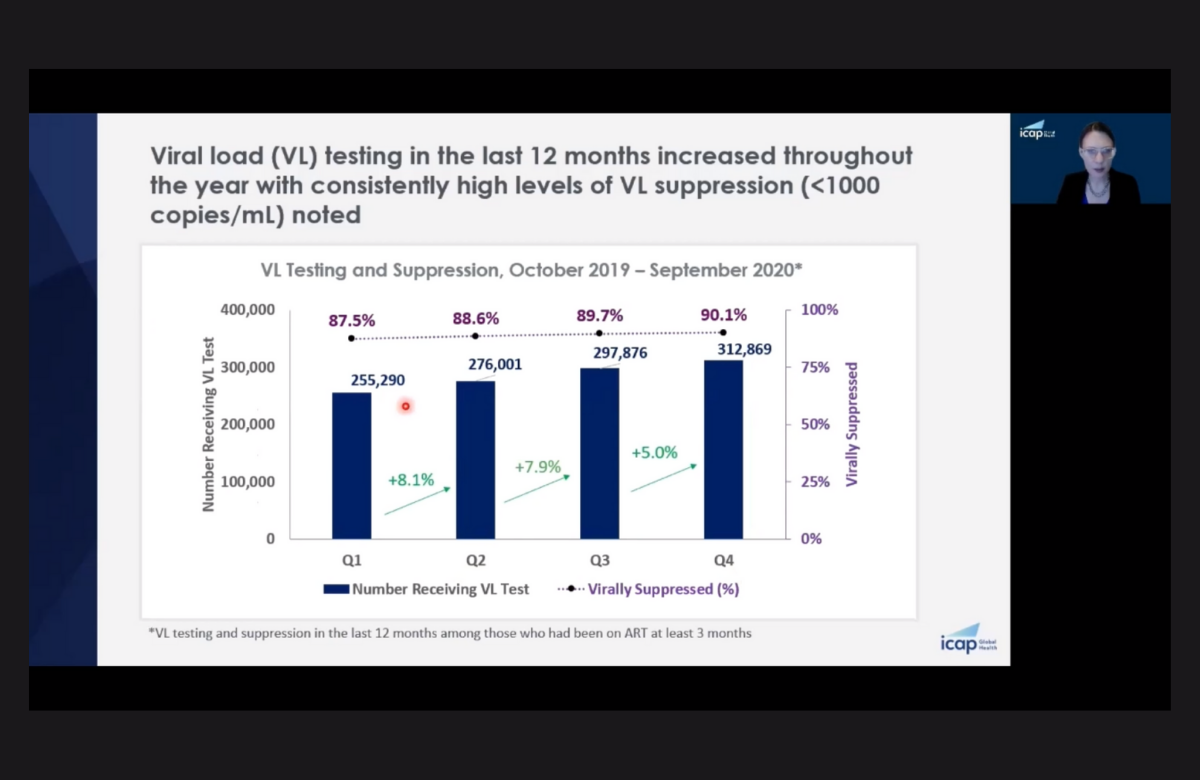 La dott.ssa Tiffany Harris durante il suo intervento a CROI 2021. | ||
|
I dati in questione sono stati raccolti tra l’ottobre 2019 e il settembre 2020 in una serie di strutture sanitarie a cui l’ICAP (Centro internazionale per i programmi di cura e trattamento dell'AIDS) della Columbia University fornisce supporto tecnico, con il finanziamento del PEPFAR (Piano di emergenza del Presidente degli Stati Uniti per la lotta all'AIDS). Le misure di contenimento per COVID-19 sono state introdotte nella maggior parte dei paesi a marzo 2020, alla fine del secondo trimestre analizzato. Rispetto al trimestre gennaio-marzo, tra aprile e giugno si è verificato un calo del 3,3% delle persone che si sono sottoposte al test HIV, un calo del 9,5% delle persone che hanno ricevuto una diagnosi positiva e un corrispondente calo del 9,8% delle persone che hanno iniziato la terapia antiretrovirale. Nel trimestre successivo (luglio-settembre) si è però assistito a una rapida inversione di tendenza: i test sono tornati ad aumentare del 10,6%, le diagnosi del 9,0% e le persone che iniziavano la terapia del 9,8%. Il numero complessivo di persone in terapia antiretrovirale non è diminuito nel corso dell'anno – anzi, è costantemente aumentato, salendo da 419.028 a 476.010. Oltre il 60% ha eseguito il test della carica virale, e anche il tasso di soppressione virale è aumentato dall'87,5% al 90,1%. | ||
Carica virale di nuovo rilevabile nel paziente di San Paolo | ||
 Il dott. Ricardo Diaz durante il suo intervento a CROI 2021. | ||
|
Nel tentativo di ridurre le dimensioni del reservoir HIV, all’uomo era stato somministrato un regime farmacologico intensificato (un mix di cinque antiretrovirali e nicotinammide), cui ha fatto seguito un'interruzione del trattamento sotto stretto controllo medico. Ad AIDS 2020 era stato riferito che il paziente non presentava tracce rilevabili né di HIV RNA né di HIV DNA, e aveva livelli esigui di anticorpi prodotti in risposta all'infezione da HIV. Pochi mesi dopo, tuttavia, le sue risposte immunitarie cellulo-mediate sono gradualmente venute meno, sono comparsi una serie di sintomi e l'RNA è tornato rilevabile. Il ceppo virale emergente presentava diverse caratteristiche genetiche rispetto a quello osservato al baseline, per ragioni che restano da chiarire. È possibile che si sia verificata un’evoluzione virale nell’organismo del paziente oppure una reinfezione con un altro ceppo; è anche possibile che il suo fosse un caso di doppia infezione e che quello emerso fosse dunque il secondo ceppo. | ||
È stata osservata un’associazione tra riassegnazione chirurgica del sesso e soppressione virologica sostenuta | ||
 La dott.ssa Cristina Rodriguez-Hart (a destra) durante il suo intervento a CROI 2021. | ||
|
In un gruppo di persone transgender di New York iscritte a Medicaid (il programma statunitense di assistenza sanitaria per persone a basso reddito) è stato osservato un aumento della soppressione virologica dopo che si sono sottoposte a riassegnazione chirurgica del sesso: è quanto si apprende da uno studio presentato a CROI 2021. L’associazione tra chirurgia di riassegnazione del sesso e aumentata soppressione virologica era già stata osservata in gruppi di popolazione che tendono ad avere bassi tassi di soppressione: neri, giovani, persone transgender provenienti da aree ad alto tasso di povertà. I ricercatori hanno confrontato i tassi di soppressione virologica in persone transgender iscritte a Medicaid che hanno ricevuto qualsiasi tipo di intervento chirurgico di riassegnazione del sesso con quelli di persone non iscritte a Medicaid e di uomini e donne cisgender. Delle 1730 persone transgender con infezione da HIV iscritte a Medicaid, quelle che si sono sottoposte a un intervento di riassegnazione del sesso nel periodo contemplato dallo studio sono poco meno dell'11%. Tra le persone transgender iscritte a Medicaid, nel periodo 2013-2017 si è registrato un aumento del 13% della soppressione virologica, con il 75% che l’ha ottenuta entro il 2017. I tassi di soppressione all’interno di questo gruppo sono tuttavia rimasti inferiore rispetto a quelli osservati nelle persone transgender non iscritte a Medicaid (83%), nelle donne cisgender (82%) e negli uomini cisgender (86%). Le persone transgender che si sono sottoposte a un intervento di riassegnazione del sesso rappresentano qui l'eccezione: nel 2017, ben l'85% di loro aveva ottenuto la soppressione virologica. In questo gruppo, il 57% degli individui era di etnia nera, il 22% aveva tra i 20 e i 29 anni e il 44% viveva in aree ad alto tasso di povertà. Il tasso di soppressione virologica è salito dal 66% due anni prima dell'intervento al 77% un anno prima, per poi arrivare all'86% un anno dopo e mantenendosi alto (88%) fino a due anni dopo l'intervento chirurgico. Secondo alcuni riscontri empirici, potrebbe esserci un legame con il fatto che in genere i chirurghi richiedono che i pazienti siano virologicamente soppressi, prima di sottoporli all’intervento. Dai dati sembra poi di poter affermare che la soppressione resti sostenuta nel tempo. In ambo gli studi, un gruppo di giovani uomini e donne transessuali di età compresa tra i 16 e i 24 anni che stavano già assumendo la terapia ormonale – metà del quale composto da donne che assumevano estrogeni e metà da uomini che assumevano testosterone – hanno poi iniziato un regime PrEP con un regime a base di tenofovir/emtricitabina a somministrazione orale, giornaliera e controllata (ossia assumendo i farmaci sotto il controllo degli operatori sanitari). Il primo studio ha esaminato i livelli di farmaci ormonali nei partecipanti, fornendo rassicurazioni sul fatto che non si abbassavano significativamente a causa della PrEP, né negli uomini né nelle donne. Il secondo si è invece concentrato sul potenziale impatto della terapia ormonale sui livelli dei farmaci PrEP. Sebbene i livelli intracellulari di tenofovir disoproxil fumarato ed emtricitabina risultassero più bassi nelle donne trans che negli uomini trans, si trattava comunque di valori compresi all'interno della gamma di quelli osservati in studi simili sulla PrEP a somministrazione controllata condotti in persone cisgender. | ||
L’impatto di TAF e inibitori dell’integrasi sull’aumento di peso | ||
 Flotsam/Shutterstock.com. | ||
|
L’assunzione di tenofovir alafenamide (TAF) è risultata correlata ad aumento di peso in tre ampi studi condotti su pazienti che effettuano lo switch a un nuovo regime di trattamento dell’HIV presentati a CROI 2021. Tutti e tre gli studi hanno identificato il TAF come fattore che contribuisce all’aumento di peso, mentre sull’impatto degli inibitori dell’integrasi i risultati sono contrastanti. Il TAF in combinazione con l'emtricitabina fa parte di molte delle combinazioni di farmaci antiretrovirali più comunemente prescritte, ed è emerso in diversi studi come un fattore di rischio indipendente per l'aumento di peso. I tre studi presentati a CROI 2021 hanno esaminato solo pazienti che effettuavano uno switch terapeutico, non considerando cioè persone che assumevano la terapia per la prima volta in modo da escludere l’effetto del “ritorno in salute” che si può osservare quando si iniziano a prendere i farmaci. Un'analisi dello studio di coorte RESPOND ha preso in considerazione 14.703 persone in Europa e Australia. I partecipanti sono stati seguiti per un periodo mediano di 2,6 anni, durante i quali poco più della metà (54%) ha registrato un aumento di peso di almeno il 7% dell'indice di massa corporea (BMI). Quattro farmaci antiretrovirali sono risultati associati ad una maggiore probabilità di aumento di peso nell'analisi multivariata: gli inibitori dell'integrasi dolutegravir e raltegravir, l’inibitore non-nucleosidico della trascrittasi inversa etravirina, e il TAF, un inibitore nucleosidico della trascrittasi inversa. Le probabilità di aumento di peso associate al dolutegravir e al TAF sono risultate più alte quando i due farmaci venivano assunti insieme, ma sia il dolutegravir che il TAF sono risultati associati in modo indipendente a più elevata probabilità di aumento di almeno il 30% del BMI. Per meglio comprendere come la assunzione pregressa di tenofovir oppure lo switch terapeutico dal TDF al TAF possano incidere sull'aumento di peso nelle persone trattate con un inibitore dell'integrasi, la prof.ssa Grace McComsey e colleghi hanno esaminato 2272 persone in carico presso i maggiori centri specializzati nell’assistenza a pazienti HIV+ negli Stati Uniti e a Londra. Tutti i partecipanti erano virologicamente soppressi e sono passati a un nuovo regime comprendente un inibitore dell'integrasi, incluso un 64% già precedentemente trattato con un altro inibitore dell'integrasi. Il 47% dei partecipanti è passato da un regime con il TDF a uno con il TAF nello stesso momento. Nei partecipanti si è registrato un aumento di peso in media di 1,3 kg nell'anno successivo allo switch, senza che vi fossero differenze in base all’inibitore dell'integrasi assunto. Sono risultate più soggette a registrare un aumento di peso almeno del 10% le donne, le persone sottopeso o normopeso al baseline, quelle che in precedenza assumevano un regime senza inibitori dell’integrasi e quelle che passavano dal TDF al TAF. Un'analisi dello studio statunitense HOPS (HIV Outpatients Study) ha mostrato che lo switch a un regime comprendente un inibitore dell’integrasi era associato all’aumento di peso in modo indipendente, e che il grosso dell’aumento di peso si verificava nei primi otto mesi dopo lo switch; dopodiché, l’eventuale ulteriore aumento di peso era in gran parte attribuibile all’assunzione del TAF. | ||
È ancora efficace dopo due anni un regime che prevede l’assunzione dei farmaci quattro giorni sì e tre no | ||
 Il dott. Roland Landman durante il suo intervento a CROI 2021. | ||
|
Un regime che prevede l'assunzione di farmaci antiretrovirali per quattro giorni consecutivi a settimana seguiti da una pausa di tre giorni si è dimostrato efficace nel mantenere la soppressione virologica quanto un regime a somministrazione giornaliera: sono i risultati alla 96° settimana di uno studio di follow-up presentato a CROI 2021. Nell'era della terapia antiretrovirale efficace, la ricerca sta indirizzando i propri sforzi verso la messa a punto di regimi che consentono alle persone HIV-positive di prendere meno farmaci. Lo studio QUATOR mirava a verificare se le persone con una carica virale non rilevabile potessero mantenere la soppressione virologica assumendo i farmaci solo quattro giorni la settimana. Se si rivelasse efficace, questo approccio non solo consentirebbe ai pazienti di fare delle pause dal trattamento, ma potrebbe anche ridurre i costi delle terapie di circa il 40%. I partecipanti allo studio assumevano vari regimi antiretrovirali. Poco meno della metà (48%) erano trattati con un inibitore dell'integrasi, più comunemente l’elvitegravir o il dolutegravir; il 46% con un inibitore non nucleosidico della trascrittasi inversa (NNRTI), più comunemente la rilpivirina; e il 6% con un inibitore della proteasi, il più delle volte il darunavir. Per le prime 48 settimane, 636 partecipanti sono stati randomizzati per continuare ad assumere il proprio regime di trattamento tutti i giorni oppure per soli quattro giorni consecutivi (dal lunedì al giovedì), seguiti da tre giorni di riposo. Dalla 48° settimana, entrambi i gruppi hanno iniziato ad assumere il trattamento quattro giorni sì e tre no per altre 48 settimane. Dopo 96 settimane, la carica virale continuava ad essere irrilevabile nel 92,7% delle persone randomizzate per l’assunzione intermittente dei farmaci fin dall’inizio e nel 96,1% di coloro che erano passate dall’assunzione quotidiana a quella intermittente. I tassi di fallimento virologico sono invece saliti rispettivamente al 4,2% e al 2,0%. Tuttavia, nel braccio con assunzione intermittente si sono osservate differenze in base ai farmaci impiegati: erano del 5,3% nei pazienti trattati con un NNRTI e del 2,4% in quelli trattati con un inibitore dell’integrasi. Sono state osservate nuove mutazioni farmacoresistenti in sette delle 19 persone che sono andate incontro a fallimento virologico sul regime intermittente. Gli autori hanno concluso che un regime che prevede l’assunzione dei farmaci quattro giorni sì e tre no ha un’efficacia che resta sostenuta a 96 settimane e un tasso di fallimento virologico ridotto, in particolare in chi è trattato con inibitori dell'integrasi. | ||
Connect with us |
||
|
NAM's news coverage of CROI 2021 has been supported by ViiV Healthcare. |
||
| Traduzione di LILA Onlus – Lega Italiana per la Lotta contro l’AIDS | ||
|
aidsmap è un’organizzazione community-based, vincitrice di numerosi premi, attiva nel Regno Unito, che fornisce in tutto il mondo informazioni accurate ed affidabili sull’HIV, a persone HIV-positive ed ai professionisti che forniscono loro cure, supporto e trattamenti.
Per maggiori dettagli, contatta aidsmap:
Tel +44 (0)20 3727 0123 Email info@nam.org.uk Web www.aidsmap.com
NAM Publications
Cally Yard, 439 Caledonian Road, London N7 9BG Company limited by guarantee. Registered in England & Wales, number: 2707596 Registered charity, number: 1011220 To unsubscribe please click here Privacy Policy: www.aidsmap.com/about-us/confidentiality |