¿Tienes problemas para leer el contenido de este correo electrónico? Puedes leerlo en tu navegador >>
|
||
 |
||
|
||
Índice
|
||
Fármacos inyectables de acción prolongada para el tratamiento y la prevención del VIH | ||
 Carlos del Rio, Diane Havlir, Charles Flexner, Francois Venter, Hyman Scott, Nittaya Phanuphak (de arriba abajo y de izquierda a derecha) durante su intervención en la CROI 2021. | ||
|
Una mesa de debate organizada dentro de la edición virtual de la Conferencia sobre Retrovirus e Infecciones Oportunistas (CROI 2021) puso de relieve la importancia de que los fármacos antirretrovirales inyectables para el VIH sean prácticos y asequibles. La profesora Diane Havlir afirmó que los avances en el tratamiento antirretroviral producidos en la última década estuvieron dominados por la aparición de la potente familia de los inhibidores de la integrasa y el desarrollo de regímenes tratamiento en un único comprimido, pero esta próxima década promete ser la de los fármacos de acción prolongada. El profesor François Venter declaró que en Sudáfrica hay un gran entusiasmo entre los pacientes por los medicamentos de acción prolongada, mientras que los profesionales sanitarios están más preocupados por los retos operativos. El exitoso programa de terapia antirretroviral de Sudáfrica es el mayor del mundo y modificarlo para adaptarlo al tratamiento inyectable supondría tener que replantear el flujo de trabajo en unas clínicas ya sobrecargadas. Venter se mostró más receptivo hacia los posibles beneficios de la profilaxis preexposición frente al VIH (PrEP) inyectable, teniendo en cuenta el limitado número de personas que, hasta ahora, han podido acceder a la PrEP oral. La primera formulación de larga duración para la PrEP (basada en cabotegravir inyectable) podría empezar a comercializarse a finales de este año o principios del próximo. No obstante, aún se ignora el coste que tendrá. Por otro lado, un análisis presentado en la CROI 2021 –realizado por la doctora Anne Neilan, del Hospital General de Massachusetts (EE UU)– concluyó que, para que dicha intervención resultara coste-efectiva en EE UU, tendría que costar menos de la mitad del precio de lista (el precio de venta sugerido por el fabricante) de la combinación inyectable de cabotegravir/rilpivirina Cabenuva (autorizada para el tratamiento del VIH). Para ser más coste-efectiva que el genérico de la combinación de tenofovir disoproxil fumarato y emtricitabina (TDF/FTC) -que cuesta 8.300 dólares al año en EE UU-, el precio de cabotegravir inyectable (CAB-LA) no debería superar los 11.600 dólares. A este precio, supondría un coste de menos de 100.000 dólares por año de vida adicional ajustado por calidad, que es el umbral máximo de lo que suele considerarse coste-efectivo en EE UU. En Europa y otros lugares, la combinación TDF/FTC genérica puede conseguirse por entre 300 y 900 dólares al año. Aunque el equipo de Neilan no lo incluyó en su análisis, el modelo implica que la mayor eficacia preventiva de cabotegravir de acción prolongada podría hacer que siguiera siendo coste-eficaz (o ahorrar costes a largo plazo) como PrEP en un escenario europeo, pero únicamente si su precio está ajustado a unos 2.000-3.000 dólares anuales. La Agencia Europea del Medicamento (EMA, en sus siglas en inglés) aprobó la combinación inyectable en diciembre de 2020, dando su respaldo tanto a un régimen de administración mensual como a uno bimestral. Sin embargo, las agencias normativas de EE UU y Canadá (donde las inyecciones se comercializan juntas como Cabenuva) solo aprobaron el régimen de administración mensual. El estudio ATLAS-2M contó con la participación de 1.045 personas que fueron distribuidas de forma aleatoria para recibir inyecciones de 400mg de cabotegravir y 600mg de rilpivirina cada cuatro semanas o de 600mg de cabotegravir y 900mg de rilpivirina cada ocho semanas. Al cabo de dos años, el 90,2% de los participantes del grupo de inyección mensual y el 91,0% del grupo de administración bimestral mantenían la carga viral indetectable. | ||
Los programas africanos del VIH mostraron su ‘resiliencia’ durante la pandemia de COVID-19 | ||
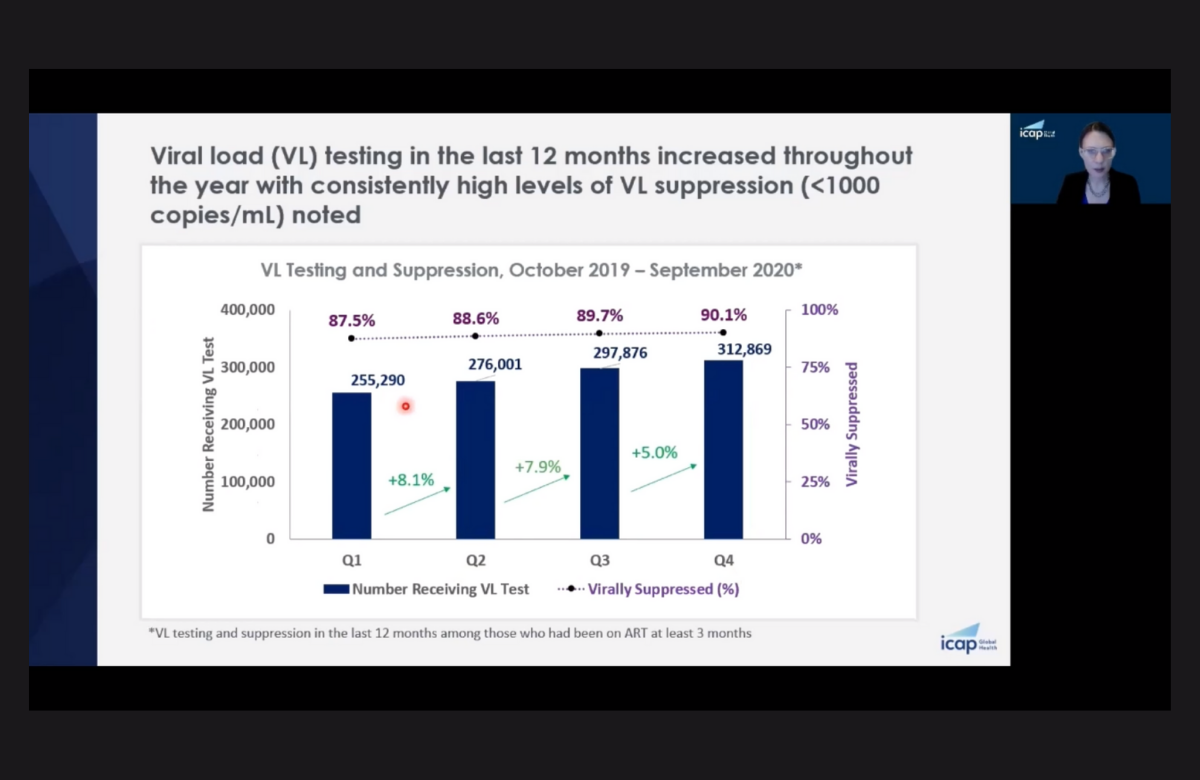 La doctora Tiffany Harris durante su presentación en la CROI 2021. | ||
|
Los datos se recopilaron entre octubre de 2019 y septiembre de 2020 en los centros de salud a los que ICAP (de la Universidad de Columbia, EE UU) presta apoyo técnico, con financiación del Plan de Emergencia del Presidente de EE UU para Paliar el Sida (PEPFAR, en sus siglas en inglés). La mayoría de los países introdujeron las medidas de control de la COVID-19 en marzo de 2020, al final del segundo trimestre analizado. Al comparar los datos de enero-marzo con los de abril-junio, se observó que se produjo un descenso del 3,3% en el número de personas que se realizaron la prueba del VIH, un descenso del 9,5% en el número de personas con un diagnóstico positivo y el correspondiente descenso del 9,8% en las personas que iniciaron el tratamiento antirretroviral. En el siguiente trimestre (julio-septiembre), se produjo un rápido repunte, registrándose un aumento del 10,6% en el número de pruebas, del 9,0% en el de diagnósticos positivos y del 9,8% en el número de personas que iniciaron su tratamiento antirretroviral. Así, el número total de personas que recibieron terapia antirretroviral no disminuyó durante el año y, de hecho, aumentó de forma constante, pasando de 419.028 a 476.010 personas. Durante ese tiempo, a más del 60% de las personas se les realizaron pruebas de carga viral y la tasa de personas con carga viral indetectable aumentó: del 87,5% al 90,1%. | ||
El paciente de São Paulo vuelve a presentar carga viral detectable | ||
 El doctor Ricardo Diaz durante su presentación en la CROI 2021. | ||
|
En un esfuerzo por reducir el tamaño de los reservorios del VIH, el hombre había recibido un régimen farmacológico intensificado (compuesto por cinco fármacos antirretrovirales, más nicotinamida) durante un tiempo antes de realizar una interrupción del tratamiento bajo estrecha supervisión. En la conferencia AIDS 2020, se informó de que presentaba niveles indetectables de ARN y ADN del VIH, así como unos niveles bajos de anticuerpos frente al VIH. Sin embargo, apenas unos meses más tarde, las respuestas inmunitarias mediadas por células desaparecieron de forma progresiva. Por otro lado, también desarrolló una serie de síntomas y volvió a tener niveles detectables de ARN viral. La cepa emergente del VIH presentaba diferencias genéticas en comparación con la cepa basal, pero aún no está claro cuál es la razón de ello. Entre las posibles explicaciones estaría la evolución viral dentro del cuerpo de esta persona, la reinfección por una nueva cepa del VIH o la reaparición de una cepa diferente de una infección doble anterior. | ||
La cirugía de afirmación de género, relacionada con el hecho de mantener una carga viral indetectable de forma sostenida | ||
 La doctora Cristina Rodriguez-Hart (derecha) durante su presentación en la CROI 2021. | ||
|
Las tasas de supresión de la carga viral entre las personas trans inscritas en Medicaid que viven en la ciudad de Nueva York (EE UU) aumentaron después de recibir la cirugía de afirmación de género, según los hallazgos de una investigación presentados en la CROI 2021. La realización de la cirugía de afirmación de género se vinculó a una mejora de las tasas de supresión viral entre los grupos que suelen tener bajas dichas tasas: personas trans jóvenes y negra que viven en zonas con grandes índices de pobreza. El equipo de investigadores comparó los resultados de las tasas de supresión de la carga viral entre las personas trans con acceso a Medicaid que recibieron cualquier forma de cirugía de afirmación de género, las de las que no tienen acceso a Medicaid y las de hombres y mujeres cis. De las 1.730 personas trans con el VIH inscritas en Medicaid, algo menos del 11% accedió a la cirugía de reafirmación de género durante el periodo de estudio. En el caso de las personas trans inscritas en Medicaid, se registró un aumento del 13% en las tasas de supresión de la carga viral entre 2013 y 2017, llegando hasta el 75% el número de personas que alcanzaron una carga viral indetectable en 2017. Sin embargo, en conjunto, las tasas de supresión de la carga viral en este grupo de población siguieron siendo inferiores a las de las personas trans no inscritas en Medicaid (83%), las de las mujeres cis (82%) y las de los hombres cis (86%). Las personas trans que se sometieron a una cirugía de afirmación de género fueron la excepción en dicha tendencia y, así, en 2017, el 85% de ellas tenía carga viral indetectable. En este grupo, el 57% eran de origen negro, el 22% tenían entre 20 y 29 años de edad y el 44% vivían en zonas con altas tasas de pobreza. La tasa de supresión de la carga viral pasó del 66% dos años antes de la cirugía al 77% un año antes. Luego aumentó al 86% un año después de la cirugía y se mantuvo en un 88% dos años después. Las pruebas anecdóticas sugieren que se suele exigir tener una carga viral indetectable antes de la operación. Los datos sugieren que la supresión de la carga viral que se consigue así, luego se mantiene en el tiempo. Dos estudios presentados en la CROI 2021 analizaron la interacción entre la terapia hormonal de afirmación de género y la profilaxis preexposición frente al VIH (PrEP). En ambos estudios, hombres y mujeres jóvenes trans de entre 16 y 24 años de edad que ya tomaban terapia hormonal (la mitad de ellos mujeres que tomaban estrógenos y la otra mitad hombres que tomaban testosterona) empezaron a tomar PrEP oral (tenofovir/emtricitabina) diaria directamente observada. El primer estudio se centró en los niveles de la terapia hormonal de afirmación de género y sus resultados ofrecieron la seguridad de que los niveles no eran significativamente más bajos, ni en hombres ni en mujeres. El segundo estudio se centró en el efecto de la terapia hormonal sobre los niveles de la PrEP. Aunque los niveles intracelulares de los fármacos de la PrEP (tenofovir disoproxil fumarato y emtricitabina) fueron más bajos en las mujeres trans que en los hombres trans, seguían estando dentro del rango observado en estudios similares de PrEP de administración mediante observación directa realizados en personas cis. | ||
¿Qué papel desempeñan tenofovir alafenamida y los inhibidores de la integrasa en el aumento de peso? | ||
 Flotsam/Shutterstock.com. | ||
|
El uso de tenofovir alafenamida (TAF) se relacionó con un aumento de peso en tres grandes estudios de personas con el VIH que cambiaban su tratamiento antirretroviral, cuyos resultados fueron presentados en la CROI 2021. Cada uno de los estudios identificó TAF como un factor que contribuía al aumento de peso, aunque arrojaron resultados contradictorios en lo que se refiere al papel de los inhibidores de la integrasa. Tenofovir alafenamida, en combinación con emtricitabina, está presente en varias de las combinaciones antirretrovirales más prescritas y su uso ha sido señalado en varios estudios como un factor de riesgo independiente de aumento de peso. Los tres estudios presentados en la CROI 2021 se centraron en personas que cambiaron de tratamiento, en lugar de personas que acababan de iniciarlo, por lo que en los hallazgos puede descartarse cualquier efecto de "retorno a la salud" debido al inicio del tratamiento. El análisis del estudio de cohorte RESPOND incluyó a 14.703 personas de Europa y Australia. Las personas participantes recibieron seguimiento a lo largo de una mediana de 2,6 años y algo más de la mitad de los participantes (54%) experimentaron un aumento de peso de al menos el 7% del índice de masa corporal (IMC). El análisis multivariable identificó cuatro fármacos antirretrovirales relacionados con una mayor probabilidad de aumento de peso: los inhibidores de la integrasa dolutegravir y raltegravir, etravirina (un inhibidor de la transcriptasa inversa no análogo de nucleósido) y TAF (un inhibidor de la transcriptasa inversa análogo de nucleótido). Aunque las probabilidades de aumento de peso asociadas a dolutegravir y TAF fueron mayores cuando los dos fármacos se utilizaron de forma conjunta, tanto dolutegravir como TAF se relacionaron de forma independiente con unas mayores probabilidades de experimentar un aumento de peso de al menos el 30% del IMC. Para investigar cómo el uso previo de tenofovir disoproxil fumarato (TDF) -o el cambio de TDF a TAF- afectaba al riesgo de aumento de peso de las personas que tomaban un inhibidor de la integrasa, la profesora Grace McComsey, junto con un equipo de colegas, analizó los datos de 2.272 personas que recibían atención del VIH en las principales clínicas de EE UU y Londres (Reino Unido). Todos los participantes presentaban una carga viral indetectable y se cambiaron a un nuevo régimen basado en inhibidores de la integrasa, incluido el 64% que había tomado previamente un inhibidor de la integrasa diferente. El 47% de las personas cambió de TDF a TAF al mismo tiempo. Los participantes ganaron una media de 1,3kg a lo largo del año siguiente al cambio, sin que se observaran diferencias en la media del aumento de peso dependiendo del inhibidor de la integrasa. El aumento de peso de al menos un 10% del IMC fue más probable en las mujeres, en las personas que presentaban un nivel basal de peso bajo o normal, en las que cambiaron de un régimen anterior que no contenía inhibidores de la integrasa y en las que cambiaron de TDF a TAF. Un análisis del Estudio de Pacientes Externos con el VIH de EE UU descubrió que el cambio a un inhibidor de la integrasa estuvo relacionado de forma independiente con un aumento de peso y que el mayor aumento de peso se producía en los primeros ocho meses tras el cambio. A partir de ese momento, el aumento de peso posterior fue atribuible en gran medida al uso de TAF. | ||
Un régimen basado en tomar el tratamiento cuatro días y descansar tres sigue mostrándose eficaz tras dos años | ||
 El doctor Roland Landman durante su presentación en la CROI 2021. | ||
|
Un régimen de tratamiento basado en tomar la medicación antirretroviral cuatro días consecutivos a la semana, seguidos por un descanso de tres días, mantuvo la supresión de la carga viral igual de bien que un régimen de administración diaria, según los resultados del seguimiento de 96 semanas presentados en la CROI 2021. En la era de la terapia antirretroviral eficaz, se están dedicando esfuerzos a conseguir que las personas con el VIH puedan tomar la medicación con menos frecuencia. El estudio QUATOR decidió comprobar si las personas con una carga viral indetectable podían mantenerla indetectable tomando la medicación únicamente cuatro días a la semana. De tener éxito, este enfoque no solo daría a las personas un descanso del tratamiento, sino que también podría reducir el coste del mismo en aproximadamente un 40%. Las personas que participaban en el estudio utilizaban distintos regímenes antirretrovirales y algo menos de la mitad (48%) tomaban un inhibidor de la integrasa (por lo general elvitegravir o dolutegravir); el 46% usaban un inhibidor de la transcriptasa inversa no análogo de nucleósido (ITINN), normalmente rilpivirina; y el 6% tomaban un inhibidor de la proteasa, por lo general darunavir. Durante las primeras 48 semanas, las 636 personas participantes fueron distribuidas de forma aleatoria para seguir tomando el mismo régimen de tratamiento diario o para tomar su medicación durante cuatro días consecutivos (de lunes a jueves), seguidos de tres días de descanso. A partir de la semana 48, ambos grupos siguieron la pauta de cuatro días de tratamiento y tres de descanso durante otras 48 semanas. A la semana 96, el 92,7% de las personas asignadas inicialmente al grupo de cuatro días y el 96,1% de las que pasaron del tratamiento diario al intermitente seguían teniendo una carga viral indetectable. Las tasas de fracaso virológico ascendieron al 4,2% y al 2,0%, de forma respectiva. Sin embargo, en el grupo de cuatro días, este valor varió en función de los fármacos utilizados: un 5,3% en el caso de las personas que tomaban un ITINN y el 2,4% en el caso de las que tomaban inhibidores de la integrasa. Se detectaron nuevas mutaciones de resistencia farmacológica en el virus de siete de las 19 personas que experimentaron un fracaso virológico con el régimen de cuatro días. El equipo de investigadores concluyó que la eficacia del régimen de administración de cuatro días de tratamiento y tres días de descanso se mantuvo a la semana 96, y se observó una tasa baja de fracaso virológico, especialmente entre las personas que tomaban inhibidores de la integrasa. | ||
Connect with us |
||
|
NAM's news coverage of CROI 2021 has been supported by ViiV Healthcare. |
||
| Traducción: Grupo de Trabajo sobre Tratamientos del VIH | ||
|
aidsmap es una galardonada organización de base comunitaria que trabaja en el Reino Unido. Proporcionamos información fiable y precisa sobre el VIH, proveniente de todo el mundo, a las personas que viven con esta infección y a los profesionales que las tratan, apoyan y cuidan.
Si deseas más detalles, puedes contactar con aidsmap
Tel. +44 (0)20 3727 0123 E-mail info@nam.org.uk Web www.aidsmap.com
NAM Publications
Cally Yard, 439 Caledonian Road, London N7 9BG Company limited by guarantee. Registered in England & Wales, number: 2707596 Registered charity, number: 1011220 To unsubscribe please click here Privacy Policy: www.aidsmap.com/about-us/confidentiality |