Se il messaggio non viene visualizzato correttamente clicca qui per consultare la versione online >>
|
||
 |
||
|
||
Contenuti
|
||
Cabotegravir/rilpivirina in formulazione iniettabile a lunga durata d’azione | ||
 La prof. Chloe Orkin durante il suo intervento a HIV Glasgow 2020 | ||
|
Lo sviluppo di farmaci per la terapia dell'HIV che garantiscono una copertura nel tempo senza dover essere assunti quotidianamente è stato uno dei temi principali della conferenza HIV Glasgow 2020, tenutasi la scorsa settimana in modalità virtuale. Diverse sono state le presentazioni incentrate sulla soluzione terapeutica iniettabile a base di cabotegravir/rilpivirina, la combinazione farmaceutica a lunga durata d’azione (o long-acting) più vicina all'approvazione da parte delle autorità regolatorie. Il cabotegravir è un inibitore dell’integrasi sperimentale, mentre la rilpivirina è un inibitore non nucleosidico della trascrittasi inversa (attualmente disponibile in forma di compressa con il nome di Edurant). I dati dello studio FLAIR, condotto su pazienti che assumevano la terapia antiretrovirale (ART) per la prima volta, hanno già dimostrato che oltre il 90% di chi riceve queste iniezioni mensili riesce ad abbattere la carica virale sotto la soglia di rilevabilità dopo 96 settimane di trattamento. A HIV Glasgow, la prof. Chloe Orkin della Queen Mary University di Londra ha presentato ulteriori dati che comprovano l’efficacia della combinazione cabotegravir/rilpivirina sia efficace indipendentemente dal fatto che i pazienti che hanno partecipato allo studio abbiano iniziato direttamente con le iniezioni o abbiano prima assunto i farmaci per via orale per quattro settimane, passando solo successivamente alla modalità iniettabile. La ragione per cui era stata prevista questa fase preliminare con somministrazione orale era garantire che i farmaci fossero ben tollerati, dal momento che gli iniettabili di tipo long-acting non possono essere rimossi in caso di problemi. Non si sono però verificati problemi di sicurezza specifici nella prima parte dello studio, senza contare che già altri farmaci iniettabili a cessione protratta, per esempio quelli psichiatrici, non richiedono una fase preliminare con somministrazione orale. Dopo 96 settimane, ai partecipanti di FLAIR che erano stati originariamente randomizzati per ricevere la ART per via orale è stato offerto lo switch terapeutico al regime a base di cabotegravir/rilpivirina. Potevano scegliere di ricevere le iniezioni immediatamente o di iniziare con le quattro settimane di somministrazione per via orale. Anche se l'assegnazione non è stata randomizzata, le caratteristiche dei 111 partecipanti che hanno ricevuto immediatamente le iniezioni e dei 121 che hanno prima assunto i farmaci per via orale erano sostanzialmente comparabili. A distanza di 24 settimane avevano ottenuto l’abbattimento della carica virale rispettivamente il 99,1% e il 93,4% dei due bracci dello studio. Un'analisi farmacocinetica non ha evidenziato differenze nelle concentrazioni dei farmaci nell’organismo a seconda se il paziente avesse o meno assunto il trattamento per via orale prima di passare alle iniezioni. Il trattamento si è dimostrato generalmente sicuro e ben tollerato. Circa un partecipante su cinque in ognuno dei due bracci ha sperimentato eventi avversi legati all’assunzione, ma si è verificato un solo evento grave, che peraltro non è stato giudicato correlato al trattamento. | ||
Disponibilità all’adesione e valutazioni di costo-efficacia dei regimi iniettabili | ||
 Immagine di Karan Bunjean/Shutterstock.com | ||
|
Stando a quanto emerge da un sondaggio condotto su 688 partecipanti in Francia, Germania, Italia e Regno Unito, due terzi dei pazienti in trattamento per l'HIV sarebbero interessati a passare a un regime iniettabile a lunga durata d’azione. I pazienti interessati allo switch terapeutico erano tendenzialmente più giovani, eterosessuali e nati all'estero, e avevano ricevuto più recentemente la diagnosi di HIV. Coloro che lamentavano specifici bisogni non soddisfatti hanno generalmente dichiarato che il regime iniettabile potrebbe rappresentare un valido aiuto: tra questi bisogni si possono ad esempio citare l’ansia all’idea di saltare per errore una dose, oppure il fastidio di essere ogni giorno costretti a ricordare di essere HIV-positivi, o le difficoltà a mantenere un’aderenza ottimale o ancora le preoccupazioni legate a questioni di riservatezza o privacy (perché per esempio si teme che l'assunzione quotidiana di pillole possa rivelare agli altri il proprio status di HIV-positivi). I ricercatori hanno intervistato anche 120 medici, che si sono detti generalmente aperti a offrire ai pazienti trattamenti iniettabili long-acting, ammesso che non costino di più. Ciò nonostante, secondo i medici solo il 26% dei pazienti sarebbero effettivamente disposti a passare a questo tipo di regime. Il sondaggio è stato condotto per conto di ViiV Healthcare, la stessa azienda che produce la formulazione iniettabile di cabotegravir/rilpivirina, quindi un risultato favorevole potrebbe non sorprendere: tuttavia, un’indagine italiana indipendente ha riscontrato un grado di interesse ancora maggiore, con l'89% degli intervistati che si sono detti interessati al regime iniettabile. Un'altra analisi presentata da ViiV ha preso invece in considerazione la questione della costo-efficacia di questi regimi, concludendo che, se il trattamento iniettabile con cabotegravir/rilpivirina migliora l'aderenza terapeutica rispetto ai farmaci a somministrazione orale, dovrebbe anche consentire un risparmio per il sistema sanitario, almeno nell’arco della vita del paziente. È anche possibile che consenta di aumentare di qualche settimana il periodo di tempo in cui il paziente con HIV che lo assume può aspettarsi di restare in buona salute e che contribuisca ad evitare qualche evento di trasmissione. Si è ipotizzato che non vi fossero differenze tra il trattamento iniettabile e quello orale in termini di efficacia biologica, e che il costo annuale del regime iniettabile fosse pari al costo medio delle tre terapie orali più diffuse. In termini di aderenza terapeutica si è invece ipotizzata una differenza: con i regimi iniettabili è infatti atteso che i pazienti si presentino agli appuntamenti in clinica con la stessa puntuale regolarità osservata nei trial clinici, mentre per le terapie orali si ipotizza che l’aderenza sia inferiore del 5-25%. È da prevedersi che la minore aderenza alle terapie orali causi, in alcuni pazienti, un aumento della carica virale sopra il livello di rilevabilità e un abbassamento della conta dei CD4, il che renderebbe necessarie terapie più costose. Supponendo che l’aderenza alle terapie orali sia del 5% inferiore, il ricorso a un regime iniettabile in 1000 pazienti consentirebbe un risparmio complessivo di 4,2 milioni di sterline (i dati sono stati calcolati per il sistema sanitario britannico). Il periodo in cui i pazienti possono aspettarsi di vivere in buona salute, invece, aumenterebbe di 43 anni per 1000 pazienti, ossia poco più di due settimane a testa in media. Infine, con un’aderenza alle terapie orali del 95% ci sarebbero dei periodi in cui i pazienti non sono virologicamente soppressi, e questo causerebbe secondo le stime due eventi di trasmissione dell’HIV in più ogni 1000 pazienti. Con livelli più bassi di aderenza alle terapie orali, il risparmio reso possibile dall’introduzione dei regimi iniettabili sarebbe ancora maggiore. | ||
Nuovo farmaco orale potrebbe essere assunto una sola volta a settimana | ||
 La dott.ssa Wendy Ankrom di Merck and Co presenta lo studio sul MK-8507 a HIV Glasgow 2020. | ||
|
Alla conferenza sono stati presentati i risultati degli studi volti alla definizione del dosaggio di un nuovo farmaco denominato MK-8507, appartenente alla classe degli inibitori non-nucleosidici della trascrittasi inversa (NNRTI), dai quali sembrerebbe di poter affermare che sia possibile somministrarlo una sola volta alla settimana. Sono stati innanzitutto condotti studi preliminari su volontari HIV-negativi, che hanno aiutato a selezionare i dosaggi da sperimentare negli studi successivi e hanno dimostrato che l'assorbimento dei farmaci non era influenzato dall’assunzione di cibo. I test successivi sono stati effettuati in volontari HIV-positivi che non avevano mai precedentemente assunto la terapia antiretrovirale. Sia con il dosaggio a 80mg che con quello a 300mg si è ottenuta una riduzione simile dei valori di carica virale – circa 1,5 logs, ossia valori 35 volte inferiori. Il MK-8507 si è mantenuto in concentrazioni superiori ai livelli minimi di efficacia per poco meno di una settimana con il dosaggio a 80mg, e per due settimane con quello a 300mg. Il dosaggio a 40mg non si è invece dimostrato altrettanto potente o in grado di garantire un’azione altrettanto prolungata. Merck & Co, la casa farmaceutica che produce l’ MK-8507, ha già allo studio un altro farmaco che può essere assunto una sola volta la settimana, l’islatravir. Sono in programma ulteriori sperimentazioni sulla somministrazione settimanale di una combinazione orale di islatravir e MK-8507 (a 80mg). Per quanto riguarda l'islatravir, in una presentazione separata a HIV Glasgow sono stati discussi i risultati a 96 settimane di uno studio di fase IIb condotto su pazienti che iniziano il trattamento dell'HIV per la prima volta. Lo studio era volto a valutare sicurezza ed efficacia della somministrazione giornaliera per via orale dell'islatravir in combinazione con l’NNRTI doravirina, che è stato messo a confronto con un trattamento a base di doravirina, tenofovir disoproxil fumarato e lamivudina, i componenti del regime monocompressa Delstrigo. A 96 settimane dall'inizio del trattamento, il 90% dei pazienti trattati con il dosaggio selezionato di islatravir più doravirina avevano ottenuto una carica virale non rilevabile, a dimostrazione che la combinazione è efficace almeno quanto un regime standard a tre farmaci. Il trattamento è anche risultato generalmente sicuro e ben tollerato. L’islatravir è adesso valutato nell’ambito di un programma di sviluppo clinico completo, con studi di fase III su pazienti che iniziano per la prima volta il trattamento, pazienti con numerosi precedenti di fallimento terapeutico e pazienti virosoppressi che effettuano lo switch da altri regimi. È in programma anche uno studio di fase II su bambini e adolescenti. Inoltre, l’islatravir è in fase di valutazione anche per l’impiego nella profilassi pre- e post-esposizione (eventualmente utilizzando dosi settimanali o mensili). I primi studi suggeriscono anche che un impianto sottocutaneo a lento rilascio di islatravir potrebbe garantire protezione per un anno. | ||
L'impatto del COVID-19 sui servizi per l'HIV in Europa | ||
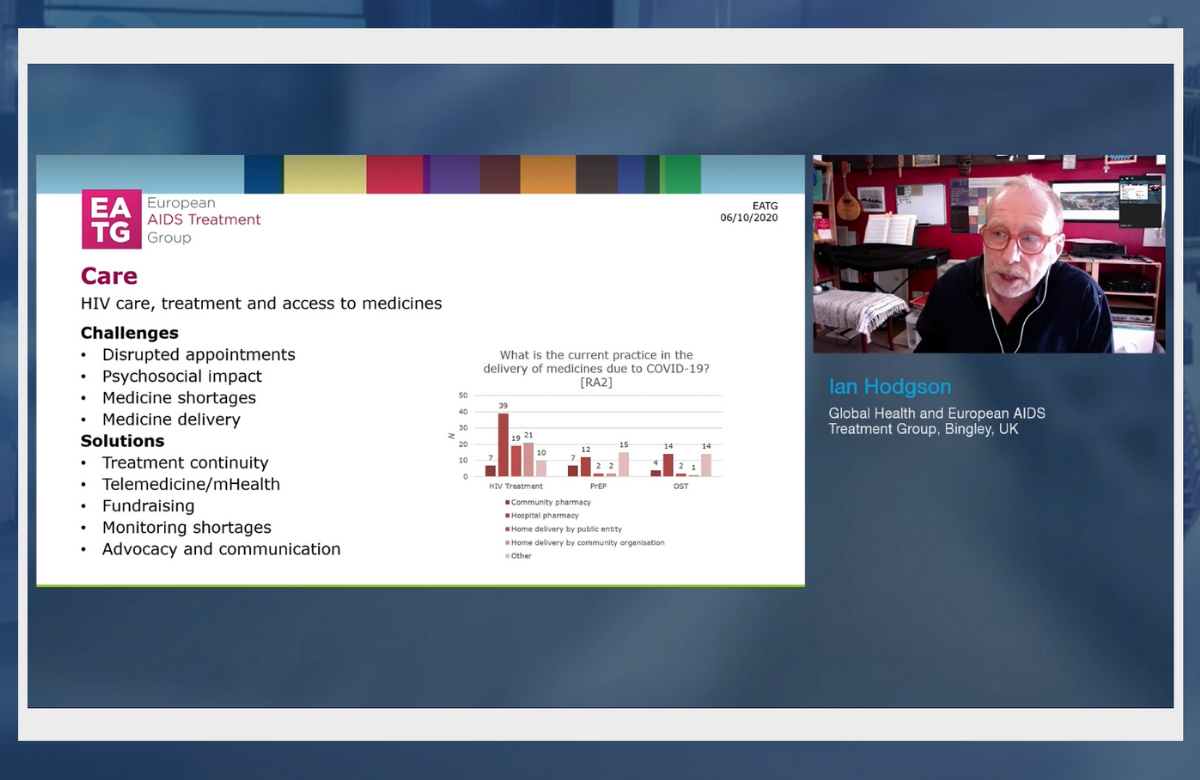 Ian Hodgson durante il suo intervento a HIV Glasgow 2020. | ||
|
Da una serie di sondaggi a risposta rapida condotti da European AIDS Treatment Group (EATG) emerge che l'accesso ai test per l'HIV, alla PrEP e al trattamento dell'HIV ha subito significativi cambiamenti nel corso dell'epidemia di COVID-19. I risultati non solo documentano gli impatti negativi, ma danno anche conto delle soluzioni innovative attuate da un certo numero di organizzazioni attive sul territorio. I servizi di offerta del test per l'HIV sembrano aver subito maggiori interruzioni della loro attività nei paesi che hanno attuato misure anti-COVID più restrittive, con l’offerta di test rapidi e servizi di prossimità spesso sospesi del tutto. Tuttavia, in molti luoghi c'è stato un aumento o almeno una non-diminuzione della disponibilità dei cosiddetti test fai-da-te, e molte ONG hanno messo in atto campagne per aumentare la conoscenza di questi strumenti diagnostici. La metà degli intervistati ha affermato che nella loro zona i test per le infezioni a trasmissione sessuale erano disponibili solo per infezioni acute ed emergenze, non per gli esami di routine. Gli intervistati provenienti da quasi tutti i paesi hanno riferito che le loro visite di controllo per l’HIV sono state in moltissimi casi posticipate, con l'invio di scorte supplementari di farmaci per la terapia antiretrovirale (ART), oppure sostituite da consulti telefonici. In alcuni paesi, il fatto che i medici hanno improvvisamente dovuto essere impiegati nell'assistenza per il COVID ha lasciato un servizio gravemente inadeguato. Dalle risposte è però anche emerso che le organizzazioni sanitarie e le associazioni attive sul territorio hanno attuato una serie di soluzioni innovative per rispondere all’emergenza, come la possibilità di ricevere prescrizioni per quantitativi di farmaci sufficienti per più tempo, o il fatto che i centri sul territorio hanno fatto le funzioni di punti di accesso al sistema sanitario sostitutivi per gli ambulatori periferici che erano stati chiusi. Alcuni operatori sanitari si sono personalmente attivati per consegnare farmaci ai pazienti, recandosi da loro con la propria auto o in bicicletta, ed è stato aumentato il numero di farmacie autorizzate ad erogare farmaci antiretrovirali. Ian Hodgson di EATG ha dichiarato alla Conferenza che per le associazioni adesso la sfida è passare da una risposta alla pandemia di COVID di tipo emergenziale a una strategica. Le priorità dei finanziatori potrebbero cambiare in modo permanente, ha affermato, e le organizzazioni potrebbero dover cambiare obiettivi e priorità per affrontare i nuovi bisogni del mondo post-COVID. | ||
L’inclusione delle donne negli studi clinici | ||
 La dott.ssa Catherine Orrell durante il suo intervento a HIV Glasgow 2020. | ||
|
La sottorappresentazione delle donne negli studi clinici è motivata dalla volontà di proteggere loro e i bambini non ancora nati dai potenziali danni causati da un farmaco, ma questo si traduce in una forma di iniquità nei confronti delle donne stesse: per la maggior parte dei nuovi farmaci non si hanno infatti dati specifici su sicurezza, efficacia e tollerabilità nella popolazione femminile. Una sessione di HIV Glasgow ha per questo approfondito gli imperativi biologici, clinici ed etici che spingono per un maggiore coinvolgimento delle donne di ogni etnia nelle sperimentazioni cliniche sull'HIV. Certe differenze biologiche hanno implicazioni cliniche, ha spiegato alla Conferenza la dott.ssa Catherine Orrell. In generale, le donne pesano meno e hanno una percentuale più alta di grasso corporeo rispetto agli uomini, il che può alterare la farmacocinetica di un farmaco nel loro organismo. Anche le fluttuazione ormonali che si verificano durante il ciclo mestruale e in gravidanza incidono sul metabolismo dei farmaci. Si consideri poi che i farmaci possono avere effetti diversi negli uomini e nelle donne: ad esempio, l’antiretrovirale nevirapina nelle donne induce epatite ed eruzioni cutanee anche con conte di CD4 molto più basse rispetto agli uomini. L'associazione del dolutegravir con l’aumento di peso nelle donne è stata scoperta solo dopo che il farmaco era stato approvato dalle autorità competenti (tale aumento di peso non era stato nemmeno registrato nei primi studi clinici). Analogamente, solo dopo l'approvazione è emersa la possibile associazione del dolutegravir con i difetti del tubo neurale, e i decisori politici hanno potuto attingere dati su questo collegamento da un unico studio, data la mancanza di altre fonti che fornissero un quadro più completo. Se le preoccupazioni di natura etica riguardo la possibilità di causare danni ai nascituri sono fondate, non si può neppure ignorare la realtà che, una volta approvati, i farmaci saranno inevitabilmente utilizzati dalle donne in gravidanza, soprattutto perché metà delle gravidanze non sono pianificate. È quindi preferibile scoprire eventuali rischi nell'ambiente controllato di una sperimentazione clinica, con le dovute precauzioni e regolamentazioni, piuttosto che utilizzare il farmaco nella pratica clinica quotidiana senza poter disporre di tali informazioni, ha fatto presente la prof. Maggie Little. Le donne con HIV in gravidanza non dovrebbero essere protette ‘dalla’ ricerca clinica, ma ‘attraverso’ la ricerca clinica, ha aggiunto la studiosa. Le donne e i loro medici devono poter disporre di dati affidabili per quanto riguarda gli aggiustamenti dei dosaggi oppure la sicurezza di un determinato farmaco sia per il feto che per la madre. L'attivista Longret Kwardem ha detto che le donne vogliono essere attivamente coinvolte in modo significativo nella ricerca, dall'inizio alla fine, e desiderano che siano condotte ricerche specifiche sulle donne attraverso tutto l’arco della loro vita, tenendo in considerazione anche la loro salute mentale e qualità della vita. | ||
L’aumento di peso in pazienti in trattamento HIV | ||
 Il prof. Andrew Carr durante il suo intervento a HIV Glasgow 2020. | ||
|
Nel suo intervento di apertura, il professor Andrew Carr del St Vincent's Hospital di Sydney ha esortato a considerare con più cautele le variazioni di grasso corporeo, ricordando come i giovani adulti HIV-negativi negli Stati Uniti arrivino ad aumentare anche di 1 kg all'anno. È vero infatti che ampi studi hanno evidenziato che, nel corso di diversi anni, le persone con HIV in trattamento antiretrovirale aumentano di peso – ma questo aumento li riporta solo a livelli non dissimili da quelli che tipicamente si osservano nelle società in cui vivono. Svariati ampi studi hanno dimostrato che l'aumento di peso mediano nelle persone che iniziano il trattamento con un inibitore dell'integrasi è in linea con l'aumento di peso medio annuo nella popolazione generale. L'aumento di peso medio, invece, può essere molto più cospicuo in questi studi, essendo il dato falsato dalla presenza di una minoranza di casi anomali interessati da forti aumenti di peso. Resta che i medici dovrebbero tenere alta l’attenzione sui casi più estremi, dacché questi individui sono più soggetti ad andare incontro a complicazioni legate al peso in futuro. Gli studi generali sulla popolazione mostrano che un aumento di 5kg/m2 nell'indice di massa corporea aumenta in modo significativo il rischio di morte. "Non c'è alcun motivo biologico per ritenere che l'obesità negli adulti HIV-positivi non comporti gli stessi rischi che nella popolazione generale", ha detto Carr. Ricordando ai delegati che ci sono voluti più di cinque anni per dimostrare con studi randomizzati che la lipoatrofia potrebbe essere prevenuta evitando gli analoghi nucleosidici della timidina, il professore ha invitato i ricercatori a cercare risposte in merito alle cause dell'aumento di peso progettando studi che potrebbero chiarire il ruolo dei singoli farmaci. Sono necessari anche studi che facciano confronti tra individui di sesso, età ed etnia diversa. Gli studi su persone che passano da un regime antiretrovirale a un altro o prendono la PrEP si attagliano maggiormente a identificare gli effetti dei singoli farmaci. Gli studi condotti su persone mai trattate in precedenza possono mostrare "gli effetti del ritorno alla salute", e l’interpretazione delle variazioni del peso corporeo è complicata dal fatto che i farmaci sono tipicamente somministrati in combinazione. Nella stessa sessione, il dott. Giovanni Guaraldi dell'Università di Modena ha affermato che distribuzione e densità del tessuto adiposo sono più importanti dell'aumento complessivo di grasso nel determinare il rischio di malattie cardiovascolari e disturbi metabolici. I pazienti con HIV che aumentano di peso dopo lo switch terapeutico a un regime contenente un inibitore dell'integrasi non guadagnano una quantità sproporzionata di grasso viscerale, che è legato a disturbi metabolici. Invece, l’aumento di massa corporea è principalmente causato dal cosiddetto grasso buono, ha detto Guaraldi. | ||
Un intervento per i disturbi del sonno | ||
 Immagine di Domizia Salusest | www.domiziasalusest.com | ||
|
Molte persone che vivono con l'HIV lamentano disturbi del sonno. Un gruppo di medici britannici ha riferito che un questionario sulla qualità del sonno già validato per altre patologie si è dimostrato uno strumento affidabile, semplice e pratico per valutare i disturbi del sonno nelle persone con HIV. Ai pazienti affetti da disturbi del sonno sono state fornite informazioni circa le buone abitudini da adottare per favorire il riposo, offrendo loro la possibilità, se opportuno, di cambiare regime antiretrovirale. A seguito di questi interventi la qualità del sonno degli interessati è migliorata, soprattutto tra coloro che hanno scelto di effettuare uno switch terapeutico da dolutegravir o un altro antiretrovirale. | ||
Sondaggio sui bollettini di NAM aidsmap
Ci piacerebbe sapere cosa ne pensi dei bollettini delle conferenze, specialmente quelli che hai ricevuto nell'ultimo anno. Ci aiuteresti rispondendo a questo breve sondaggio? Sarà molto utile come feedback per i nostri finanziatori. Il sondaggio (in inglese) richiede non più di 5-10 minuti per essere compilato. | ||
Connect with us |
||
|
NAM's news reporting services from HIV Glasgow 2020 have been made possible thanks to support from Gilead Sciences Europe Ltd, ViiV Healthcare and the organising committee of the HIV Glasgow conference. |
||
| Traduzione di LILA Onlus – Lega Italiana per la Lotta contro l’AIDS | ||
|
aidsmap è un’organizzazione community-based, vincitrice di numerosi premi, attiva nel Regno Unito, che fornisce in tutto il mondo informazioni accurate ed affidabili sull’HIV, a persone HIV-positive ed ai professionisti che forniscono loro cure, supporto e trattamenti.
Per maggiori dettagli, contatta aidsmap:
Tel +44 (0)20 3727 0123 Email info@nam.org.uk Web www.aidsmap.com
NAM Publications
Cally Yard, 439 Caledonian Road, London N7 9BG Company limited by guarantee. Registered in England & Wales, number: 2707596 Registered charity, number: 1011220 To unsubscribe please click here Privacy Policy: www.aidsmap.com/about-us/confidentiality |